
Cardiovalve presenta el expediente CE para su aprobación tras la finalización exitosa del estudio TARGET
Datos prometedores sobre el dispositivo de reemplazo de la válvula tricúspide Cardiovalve presentados en la reunión PCR London Valves 2025
LONDRES, 17 de noviembre de 2025/PRNewswire/ -- Venus Medtech (Hangzhou) Inc. (2500.HK) anunció hoy que Cardiovalve ha presentado el expediente técnico CE para su sistema de reemplazo de válvula tricúspide transcatéter (TTVR) ante DEKRA, el organismo notificado responsable de la aprobación de la marca CE en Europa. Este hito se produce tras la finalización exitosa del estudio TARGET, en el que participaron 150 pacientes y se demostró la seguridad y el rendimiento del sistema Cardiovalve.
Los resultados provisionales del estudio TARGET: "Seguridad y rendimiento del sistema de reemplazo de válvula cardiovascular para la regurgitación tricuspídea" fueron presentados ayer por el profesor Georg Nickenig, en nombre de los investigadores del estudio TARGET, durante la sesión de ensayos clínicos de última hora en el pabellón principal de PCR London Valves.
El estudio TARGET realizó un seguimiento a 150 pacientes en 30 centros de Europa, Reino Unido y Canadá como parte de un ensayo clínico prospectivo, de un solo brazo, abierto y multicéntrico, diseñado para evaluar la seguridad y el rendimiento del sistema Cardiovalve TR.
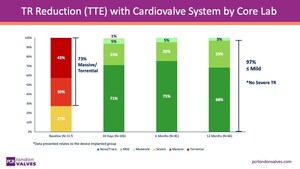
Los resultados provisionales del estudio, publicados el 16 de noviembre de 2025, mostraron que el reemplazo de la válvula tricúspide por vía transcatéter (TTVR) con el sistema Cardiovalve eliminó eficazmente la regurgitación tricúspide (RT) en la mayoría de los pacientes, a pesar de que el 73% presentaba RT masiva o torrencial al inicio del estudio, lo que demuestra la eficacia clínica del dispositivo en los pacientes.
Además de los criterios de valoración de eficacia, se observó que el procedimiento tenía un perfil de seguridad aceptable, con mejoras en los síntomas de los pacientes a los 30 días posteriores al tratamiento.
Los pacientes inscritos en el estudio continuarán en seguimiento durante un máximo de cinco años. Próximamente se presentarán los resultados clínicos y ecocardiográficos completos, incluyendo la mortalidad y las hospitalizaciones por insuficiencia cardíaca de la cohorte completa de 150 pacientes.
El profesor George Nickenig afirmó: "Los resultados del estudio Cardiovalve son muy alentadores, ya que demuestran una gran eficacia en la reducción de la insuficiencia tricuspídea (IT) y un perfil de seguridad favorable, especialmente con la nueva versión del dispositivo. Estos hallazgos representan un importante avance y ofrecen la esperanza de que los pacientes que sufren de IT pronto tengan acceso a una opción de tratamiento novedosa y eficaz".
"La presentación del expediente CE marca un hito fundamental y acerca a Cardiovalve a ofrecer una terapia transformadora para pacientes con insuficiencia mitral y tricuspídea grave", declaró Amir Gross, consejero delegado de Cardiovalve. "Este logro refleja el compromiso de un equipo comprometido con una visión compartida, un equipo que no solo se propone metas, sino que las alcanza. Nuestro más sincero agradecimiento a los investigadores, coordinadores, socios clínicos y, sobre todo, a los pacientes y sus familias por su confianza".
Lim Hou-Sen, consejero delegado de Venus Medtech , explicó: "Estos prometedores resultados marcan un avance significativo para los pacientes que sufren de insuficiencia tricuspídea. Con la solicitud de marcado CE en revisión, Cardiovalve está bien posicionada para obtener la certificación e iniciar el lanzamiento comercial del sistema TR para 2027".
Acerca de Cardiovalve
Cardiovalve, filial de Venus Medtech , es pionera en la tecnología de reemplazo valvular transcatéter y líder en innovación para el tratamiento de cardiopatías estructurales. Con más de 150 patentes aprobadas, un equipo altamente experimentado y una planta de fabricación de última generación, Cardiovalve se dedica a ofrecer a los médicos soluciones innovadoras que mejoran los resultados y la calidad de vida de los pacientes, sin necesidad de cirugía a corazón abierto.
Acerca de Venus Medtech
Venus Medtech (Hangzhou) Inc. (2500.HK) es una empresa líder e innovadora en soluciones de válvulas cardíacas transcatéter para cardiopatías estructurales. La compañía ha desarrollado una amplia gama de productos que abarcan las cuatro válvulas cardíacas: TAVR, TPVR, TMVR y TTVR, así como productos accesorios relacionados. Con centros de I+D en China, Estados Unidos e Israel, la compañía está comprometida con ofrecer soluciones de tratamiento eficaces para enfermedades potencialmente mortales.
Foto - https://mma.prnewswire.com/media/2824126/TR_Reduction__TTE__Cardiovalve_System_Core_Lab.jpg






Share this article