
Cardiovalve reicht nach erfolgreichem Abschluss der TARGET-Studie CE-Antrag zur Zulassung ein
Auf der PCR London Valves 2025 Konferenz wurden interessante Daten zum Cardiovalve-Trikuspidalklappenersatzgerät vorgestellt.
LONDON , 17. November 2025 /PRNewswire/ -- Venus Medtech (Hangzhou) Inc. (2500.HK) hat heute bekannt gegeben, dass Cardiovalve die technischen Unterlagen für sein Transkatheter-Trikuspidalklappenersatzsystem („Transcatheter Tricuspid Valve Replacement", TTVR) bei DEKRA, der für die CE-Kennzeichnung in Europa zuständigen benannten Stelle, eingereicht hat. Dieser Meilenstein folgt auf den erfolgreichen Abschluss der TARGET-Studie, an der 150 Patienten teilnahmen und die die Sicherheit und Leistungsfähigkeit des Cardiovalve-Systems nachwies.
Die vorläufigen Ergebnisse der TARGET-Studie: „Sicherheit und Leistung des Cardiovalve-Ersatzsystems bei Trikuspidalinsuffizienz" wurden gestern von Prof. Georg Nickenig im Namen der TARGET-Studienleiter während der Sitzung „Top Late-Breaking Trials" in der Main Arena der PCR London Valves vorgestellt.
Die TARGET-Studie begleitete 150 Patienten an 30 Standorten in Europa, Großbritannien und Kanada im Rahmen einer prospektiven, einarmigen, offenen, multizentrischen klinischen Studie, die zur Bewertung der Sicherheit und Leistungsfähigkeit des Cardiovalve TR-Systems konzipiert wurde.
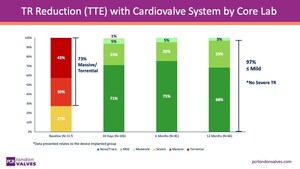
Die am 16. November 2025 veröffentlichten Zwischenergebnisse der Studie zeigten, dass der Transkatheter-Trikuspidalklappenersatz (TTVR) mit dem Cardiovalve-System bei der Mehrheit der Patienten die Trikuspidalinsuffizienz (TR) wirksam beseitigte, obwohl 73 % zu Beginn der Studie eine massive oder schwere TR aufwiesen, was die klinische Wirksamkeit des Geräts bei Patienten belegt.
Zusätzlich zu den Endpunkten für die Wirksamkeit wurde beobachtet, dass das Verfahren ein akzeptables Sicherheitsprofil aufweist und die Symptome der Patienten 30 Tage nach der Behandlung verbessert waren.
Die an der Studie teilnehmenden Patienten werden bis zu fünf Jahre lang weiter beobachtet. Umfassende klinische und echokardiographische Ergebnisse, einschließlich Mortalität und Krankenhausaufenthalten aufgrund von Herzinsuffizienz aus der gesamten Kohorte von 150 Patienten, werden in Kürze vorgestellt.
Prof. George Nickenig sagte : „Die Ergebnisse der Cardiovalve-Studie sind sehr ermutigend und zeigen eine starke Wirksamkeit bei der Reduzierung der Trikuspidalinsuffizienz (TR) und ein günstiges Sicherheitsprofil, insbesondere mit der neuen Geräteversion. Diese Ergebnisse stellen einen wichtigen Fortschritt dar und geben Hoffnung, dass Patienten, die an TR leiden, bald Zugang zu einer neuartigen und wirksamen Behandlungsoption haben werden."
„Die Einreichung des CE-Dossiers stellt einen entscheidenden Meilenstein dar und bringt Cardiovalve der Bereitstellung einer transformativen Therapie für Patienten mit schwerer Mitral- und Trikuspidalinsuffizienz einen Schritt näher", erklärte Amir Gross, Geschäftsführer von Cardiovalve. „Diese Errungenschaft spiegelt das Engagement eines fokussierten Teams mit einer gemeinsamen Vision wider, eines Teams, das nicht nur Ziele setzt, sondern diese auch erreicht. Unser tiefster Dank gilt den Forschern, Koordinatoren, klinischen Partnern und vor allem den Patienten und ihren Familien für ihr Vertrauen."
Lim Hou-Sen, CEO von Venus Medtech, erklärte: „Diese vielversprechenden Ergebnisse stellen einen bedeutenden Fortschritt für Patienten mit Trikuspidalinsuffizienz dar. Mit der zur Prüfung eingereichten CE-Zulassung ist Cardiovalve gut positioniert, um die Zertifizierung zu erhalten und bis 2027 mit der kommerziellen Einführung des TR-Systems zu beginnen."
Informationen zu Cardiovalve
Die Tochtergesellschaft von Venus Medtech, Cardiovalve, ist ein Pionier im Bereich der Transkatheter-Klappenersatztechnologie und steht an der Spitze der Innovation in der strukturellen Herztherapie. Mit mehr als 150 zugelassenen Patenten, einem sehr erfahrenen Team und einer hochmodernen Produktionsstätte hat sich Cardiovalve zum Ziel gesetzt, Ärzten Lösungen der nächsten Generation anzubieten, die die Behandlungsergebnisse und die Lebensqualität der Patienten verbessern – ohne dass eine Operation am offenen Herzen erforderlich ist.
Informationen zu Venus Medtech
Venus Medtech (Hangzhou) Inc. (2500.HK) ist ein führender Innovator bei Transkatheter-Herzklappenlösungen für strukturelle Herzerkrankungen. Das Unternehmen hat eine umfassende Produktpipeline entwickelt, die alle vier Herzklappen - TAVR, TPVR, TMVR und TTVR - sowie zugehörige Zubehörprodukte abdeckt. Das Unternehmen verfügt über globale Forschungs- und Entwicklungszentren in China, den Vereinigten Staaten und Israel und hat sich zum Ziel gesetzt, wirksame Behandlungslösungen für lebensbedrohliche Krankheiten anzubieten.
Foto - https://mma.prnewswire.com/media/2824126/TR_Reduction__TTE__Cardiovalve_System_Core_Lab.jpg






Share this article